��Դ���������ڣ�2021-12-06(1378)
��������Cervical cancer����������Ů�Եĵڶ���֢ɱ�֣����������ʦ���ߵİ�֢֮һ��
ȫ��Χ�ڣ�ƽ��ÿ2���Ӿ���һ��Ů�������ӹ���������һ��Ĺ������������������ء�����
2020���й��������·�������11������������6�ֱ�Լռȫ��������������18.3%��17.6%���ҹ�����������Լ�|ռȫ���1/5������ѹ���ܴ�
��������Ҳ��Ŀǰ�������а�֢�У�Ψһ����ͨ������Ԥ������������İ�֢��
ȫ��Χ���о������ʾ��99.7%�Ĺ�������������ͷ��������Human Papillomavirus��HPV����Ⱦ�йأ��������Եĸ�Σ��HPV��Ⱦ���ǵ��¹�����Ƥ�����估����������Ҫԭ��[1]�����������ٴ�ͨ������HPV DNA�����Ϊ��������ɸ�ķ�������ʵ�����֣�HPV DNA����ٴ���������ƫ���ߣ����������߿ֻţ��������¹������[2]������о����֣�HPV E6/E7 mRNA����ٴ��ء����Ը��ߣ��������ɸ��Ч�ܣ�ʹ���ߨ�����[3]��
HPV������ͷ���������ƣ���һ��С���Ө��Ļ�״˫��DNA�����������鳤Լ8000����ԣ�bp������Ϊ3����������������ת¼����E���������ڡ�ת¼����L�����ͷ�ת¼��������������LCR��������E����E6��E7�������������°����ף��ǵ��¹���������Ҫԭ��[4]��
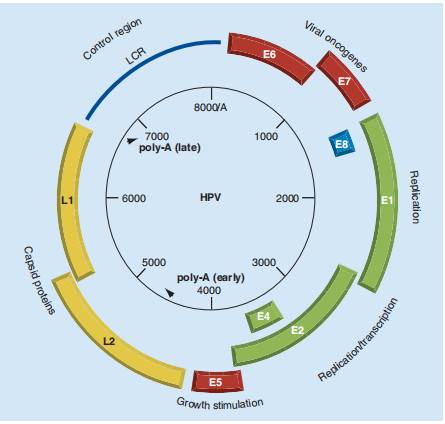
ͼ1��HPV����������ṹ
�ڸ�Σ��HPV��ʼ��Ⱦ�Σ�HPV E6/E7�����ھ�Ĭ�ڣ��������ͱ���HPV E6/E7 mRNA��һ�㲻����������ף����������������սϵͣ�һ���Ը�Ⱦ��ദ�ڴ˽Σ�����Σ��HPV���������Ⱦ��ʱ��HPV E6/E7 mRNA��ˮƽ���ء�����������ף�������չΪ��ǰ���䣬ֱ������[5-6]����ˣ�HPV E6/E7 mRNA�Dz��������Ծ״̬�Ĺؼ��Ա�־���HPV�Ħ� �²����������Ź�������Ŧ������HPV E6/E7 mRNA�����Ը������ɸ��ͷ���HPV����Ĺ�����Σ�������һ���Ը�Ⱦ��
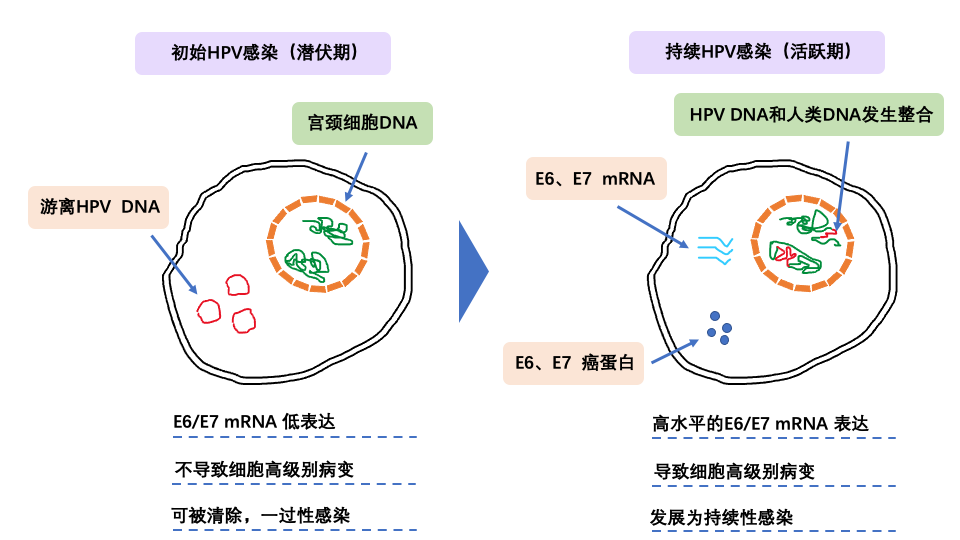
ͼ2��HPV��Ⱦ����
ɸ���HPV DNA���Ի�����ν��з�������Ҫ��Ŀǰϸ��ѧ�Ѳ���ĿǰΨһ����ѡ�e�����ֶΡ�HPV E6/E7mRNA�ɴӰ���������Ծ״̬�����Ϸ���������������ϸ��ѧ�����������ٴ��о�����mRNA���ڷ���HPV DNA ���Ի����ǿɿ��������[7]��
2015��ŷ������ɸ��ָ��ָ����HPV DNA���HPV�����������Ƿ���ڣ���HPV E6/E7 mRNA����방֢��չ��ػ���ı��������Ч����һ���Ը�Ⱦ�ļ������ʱ���ֹ������������սϸߵĻ��ߣ����HPV E6/E7 mRNA�������ṩ�����ʵ�������[8]��
2019����������������������ѧ�ᣨAmerican Society for Colposcopy and Cervical Pathology��ASCCP��������ɸ��ָ���Ƽ����ڷ��������ķ�ʽ���Բ�ͬ������Ⱥ���ò�ͬ�Ĺ������ԣ�����֧�־߱����������ԵIJ�Ʒ�����ڹ�����ɸ�飬���а���HPV E6/E7 mRNA��ⷽ����9�ݡ�
����HPVɸ��Ĺ㷺�ռ���HPV E6/E7 mRNA�ڹ�����ɸ�鷽��ļ�ֵ�õ��ˡС�������о�����֤�������ٴ������HPV DNA����HPV E6/E7 mRNA�����ٴ������Ⱥ������Խ����˶Ա��о����о����������HPV E6/E7 mRNA�����HPV DNA���������Ƶ������ԣ���HPV E6/E7 mRNA��������Ը��ߣ�10-11�ݡ�
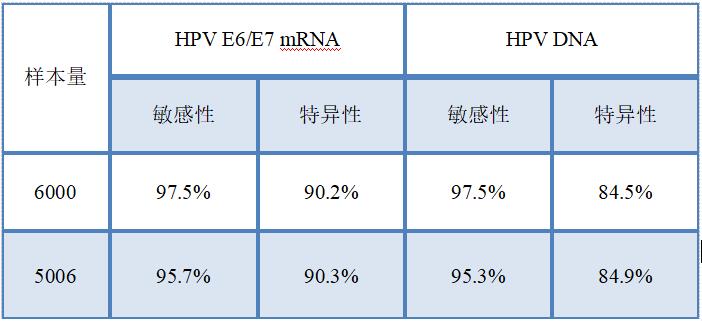
��1��HPV DNA��HPV E6/E7 mRNA�ٴ�ɸ�������Ⱥ������ԶԱ�
Ӣ��һ���о���ʾ���������HPV E6/E7 mRNA������HPV DNA��⣬����ʹ����Ҫ��������������28009�Σ�����Ҫ��HPV DNA������90605�Σ�����Ҫ��ϸ��ѧ������253477�Σ�ɸ����ÿ��Խ�ʡ1500����Ӣ����12�ݡ�
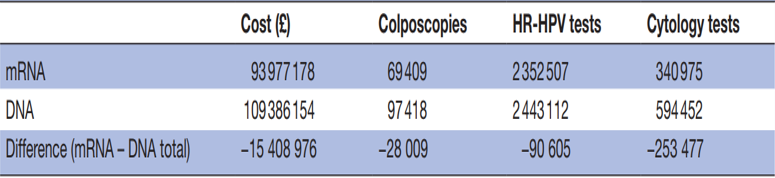
��2��HPV DNA��HPV E6/E7 mRNA�ٴ�ɸ���ֵ�Ա�
����������HPV E6/E7 mRNA��Ϊָʾ����������ת¼���ڻ�Ծ״̬�ķ��ӱ�־��ٴ���������Ը��ߣ����Խ�һ�������ɸ���п��ܷ�չΪ��֢�Ĺ�����ǰ���䣬�����ɡ�һ����HPV������Ⱦ���µ����Բ���ļ��������ƣ����Ỽ������ѹ�������ͻ������Ƴɱ���ʹ�������档
��˾��Ʒ����MPA��⼼���������ڼ��HPV16��18��31��33��35��39��45��51��52��56��58��59��66��68��14�ָ�Σ��HPV E6/E7mRNA������������������14��HPV E6/E7 mRNA�IJ�Ʒ��
�����������ƣ�
1����������ԶȲ�����100����/��Ӧ��
2��������ݣ���������ȡ����ü�ⱨ��ʱ��������3Сʱ��
3�����ݳ���4ͨ��ӫ��PCR��
4��������������
5���������Դ���ʿأ����ʿؼ�������RNA���ɶԼ�������ת¼��������������������ȫ�̼�ء�
1) ����ҩƷ�ල������. ����ͷ��������HPV�������⼰������͡��Լ��������ָ��ԭ��2015���93��ͨ�棩.
2) Li Liu,et al.Role of E6/E7 mRNA in discriminating patients with high-risk human papilloma virus-positive associated with cytology-negative and atypical squamous cells of undetermined significance��J��.Biomedical Research . 2017��28��9����3986-3990.
3) Mockel J,et al. Human Papillomavirus E6/E7 mRNA testing has higher specificity than liquid-based DNA testing in the evaluation of cervical intraepithelial neoplasia. Anal Quant Cytol Histol. 2011 Dec;33(6):311-5.
4) Lie AK, et al. Human papillomavirus E6/E7 mRNA testing as a predictive marker for cervical carcinoma. Expert Rev Mol Diagn. 2008 Jul;8(4):405-15.
5) M Thomas, et al. Human papillomaviruses, cervical cancer and cell polarity [J] .Oncogene (2008) 27, 7018�C7030.
6) ���Ҳ�. ��Σ��HPV DNA�������������ϼ��°�����������о���չ. �ִ������ƽ�չ, 2015, 24(5):384-386.
7) 2015 European guidelines for quality assurance in cervical cancer screening P62.
8) 2019 ASCCP Risk-Based Management Consensus Guidelines for Abnormal Cervical Cancer Screening Tests and Cancer Precursors .
9) J Cuzick, et al. Comparing the performance of six human papillomavirus tests in a screening population[J]. British Journal of Cancer, 2013.
10) Monsonego J , et al. Risk assessment and clinical impact of liquid-based cytology, oncogenic human papillomavirus (HPV) DNA and mRNA testing in primary cervical cancer screening (The FASE Study)[J]. Gynecologic Oncology, 2012, 125(1):175-180.
11) Weston G , Dombrowski C , Harvey M J , et al. Original research: Use of the Aptima mRNA high-risk human papillomavirus (HR-HPV) assay compared to a DNA HR-HPV assay in the English cervical screening programme: a decision tree model based economic evaluation[J]. BMJ Open, 2020, 10(3).